Lien vers la présentation du projet :
Archives de catégorie : promo133
Les matériaux supramoléculaires
Dans le cadre des projets scientifiques, Victoria, Gauthier et moi avons eu l’opportunité de travailler sur les propriétés rhéologiques des matériaux supramoléculaires. Ces derniers sont un domaine encore peu exploré mais qui intéresse le monde scientifique car il permet de former des polymères grâce à des liaisons hydrogènes qui se réorganisent très rapidement.
Nous nous sommes intéressés à deux molécules en particulier: l’EHUT et le PDMSUT.
La vidéo ci-dessous présente un aperçu des résultats que nous avons obtenus:
La fiche méthode téléchargeable par le lien ci-dessous vous permettra de comprendre les manipulations réalisées:
Protocoles et méthodes
Nous tenons à remercier tout particulièrement Guylaine Ducouret pour son accompagnement et sa patience, Laurent Bouteiller pour son aide précieuse, les laboratoires du SIMM et du PMMH, ainsi que les encadrants des PSE.
Synthèse d’un moule « Type graphène » nanostructuré
Le graphène est un matériaux d’avenir. Ses propriétés mécaniques, chimiques et électroniques sont incroyables, et sa composition en fait une ressources inépuisable (avantage majeur par rapport aux métaux).
Cependant, sa fabrication est complexe, et chère. Il y a donc une nécessité de trouver de nouvelles voies de synthèse, ou de s’inspirer de cette structure afin de créer de matériaux analogues.
C’est là que démarre notre projet: l’étude de molécules appelées « alcanes semi-fluorés » (utilisés à l’origine comme sang artificiel) a permis de mettre en évidence leur auto-assemblage à la surface de l’eau. Celle-ci forment en effet un patern hexagonale, de taille nanométrique. Les chercheurs nous ont alors confié leur idée: utiliser ceci comme un moule, pour créer une structure en nid d’abeille (pseudo graphène) en argent.
C’est ainsi qu’à démarré notre aventure:
Pour un public souhaitant un coté scientifique approfondi:
Pour tout renseignements supplémentaires:
gaetan.grimaldi-desdra@espci.fr
Blown Air Effect
Percolation optique
Filtration et bouchage en milieu complexe
Soft Robotics – Conception d’un nageur autonome en polymère électrostimulable
Vidéo de présentation de notre projet
Pour une approche plus détaillée du projet, voir la présentation du 17 juin 2016.
Presentation
Protocoles & Méthodes
Synthèse des hydrogels
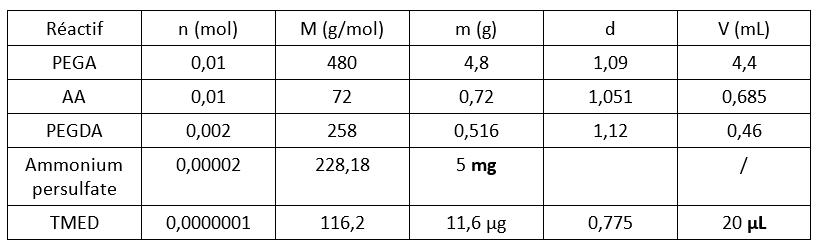
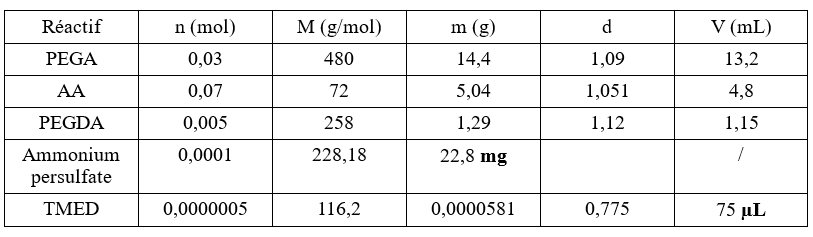
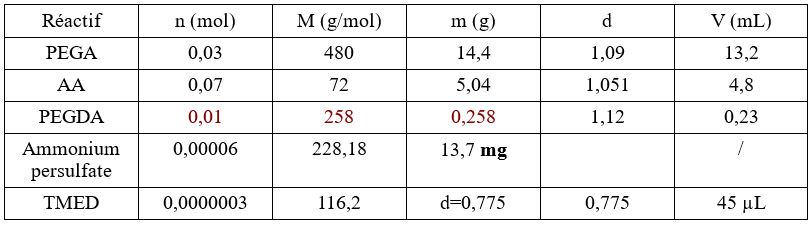
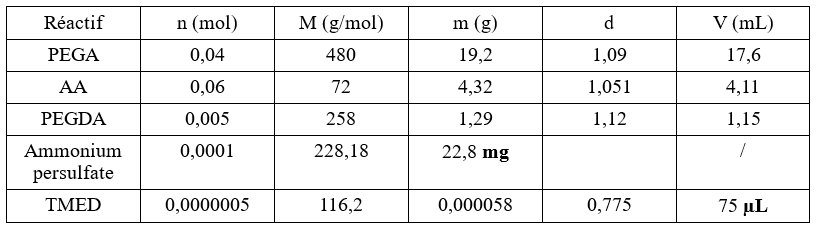
L’hydrogel utilisé est un copolymère d’acide acrylique (AA) et de polyéthylène glycol acrylate (PEGA) chimiquement réticulé par le polyéthylène glycol diacrylate (PEGDA). La différence entre les différents protocoles réside essentiellement dans la modification du ratio entre les deux monomères utilisés.
Toutes les manipulations se font sous hotte.
Dans un erlenmeyer placé sous agitation, on dissout 5mg de soude dans 10mL d’eau distillée (pH=12). On introduit successivement le PEGA, l’AA et le PEGDA. On ajoute quelques gouttes d’éosine ou de bleu de méthylène pour colorer la solution. On ajoute le persulfate d’ammonium et le TEMED pour amorcer la polymérisation. On introduit rapidement la solution dans des pipettes en plastique. On couvre le dessus des pipettes de parafilm et on laisse la solution gélifier dans une étuve à 60°C durant 10h.
PEGA/AA/PEGDA : 1/1/0,2 (monomères/réticulant : 1/0,1)
PEGA/AA/PEGDA : 1/2,3/0,17 (monomères/réticulant : 1/0,05)
PEGA/AA/PEGDA : 1/2,3/0,3 (monomères/réticulant : 1/0,1)
PEGA/AA/PEGDA : 1/1,5/0,125 (monomères/réticulant : 1/0,05)
Expérience de déflexion et d’oscillation de l’hydrogel
Matériel
– fil électrique
– une relai électrique DPDT
– un générateur de tension basses fréquences
– une cuve
– un support
– une source de tension réglable (un générateur d’électrophorèse par exemple)
– deux lames d’acier inoxydable
– du parafilm
– un réchaud
– deux feuilles de graphite
– un peigne
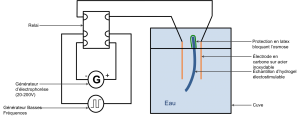
Montage
La cuve est remplie d’eau, ou d’une solution saline de concentration contrôlée inférieure à 10-1M. Les électrodes sont placées dans les crans du peigne prévus à cet effet. L’échantillon de polymère est placé dans le cran central du peigne, et la partie supérieure de l’hydrogel est isolée de la solution par un système d’enveloppe (doigt de gants de protection ici).
Cuve, peigne et support
La cuve est façonnée de PMMA. Une grille de dimension connue peut être tracée sur le fond de la cuve pour servir de repère.
Le peigne comporte une ouverture centrale destinée à accueillir l’hydrogel du test. Des crans, servant à accueillir les électrodes, sont régulièrement espacés à partir de l’ouverture centrale. Ils permettent de s’adapter au mieux à la géométrie du mouvement, et de moduler le champ électrique appliqué entre les électrodes.
Le support sert à placer une caméra pour l’acquisition d’image à analyser. Pour augmenter le contraste, et donc exploiter plus facilement les images, on peut placer la cuve sur une plaque à LED.
Fabrication des électrodes inertes
– faire chauffer deux lames d’acier inoxydable à une température de 60°C.
– sur les deux lames chaudes, superposer successivement une couche de parafilm et un feuillet de graphite.
– compresser le tout jusqu’à ce que l’électrode ait refroidi à température ambiante.
Les électrodes ainsi construites sont prêtes à l’emploi, il suffit de les connecter à une source de tension en utilisant des pinces croco ou en soudant la face carbonée à un fil dénudé avec de l’étain.
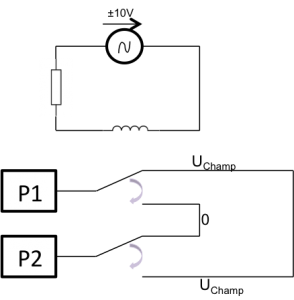
Fonctionnement du relais
Sous l’action d’un champ magnétique, généré pas la self et contrôlé par le GBF, ce device inverse l’orientation du champ électrique entre les électrodes. On crée ainsi un champ électrique d’amplitude montant jusqu’à 200V.
Protocole
– Placer une caméra sur le support au dessus de la cuve.
– Placer les électrodes aux crans souhaités.
– Placer l’hydrogel à tester
– Filmer les oscillations du polymère pour une fréquence et une tension donnée
– Faire varier les paramètres de tension et de fréquence
Les images expérimentales peuvent ensuite être traitée sous ImageJ pour en extraire amplitude d’oscillation et vitesse d’oscillation.
Électronique
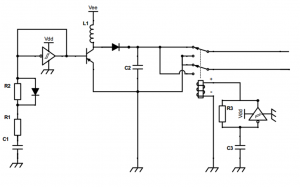
Schéma du montage électronique
Vee = 6 V
Vdd = 6 V
R1 = 15 Ω
R2 = R3 = Résistance variable 100 Ω – 5 MΩ
C1 = 10 nF
C2 = 1 µF (haute tension)
C3 = 10 µF
L1 = 6800 µH
Remarques
Vee est la tension à amplifier, Vdd est l’alimentation des triggers de Schmitt. En pratique, on soude deux piles boutons de 3 V en série pour avoir une tension d’alimentation Vdd > 5V nécessaire pour le fonctionnement du trigger de Schmitt. Les mêmes piles sont utilisées pour alimenter les deux triggers de Schmitt : un composant contient 4 triggers de Schmitt qui sont reliés aux deux mêmes pattes d’alimentation.
R2 et R3 sont des résistances variables pour avoir plus de flexibilité pour fixer l’amplification réalisée par le hacheur et la fréquence d’oscillation. Une fois la valeur optimale trouvée, on peut les remplacer par des résistances à valeur fixe.
C2 doit pouvoir supporter la tension de sortie de l’ordre de 100V. Il faut veiller à utiliser un matériel adapté : les condensateurs « classiques » ne supportent pas de telles tensions a priori.
Réalisations
Nous avons réussi à obtenir une fréquence d’oscillation minimale de 2 Hz. Elle est facilement ajustable en remplaçant la capacité C3 et/ou la résistance R3.
En ce qui concerne l’amplification, nous avons réussi à amplifier 6V en 60V. On pourrait espérer obtenir une meilleure amplification avec une optimisation des valeurs des composants. Ceci étant, nous avons réussi à obtenir un mouvement satisfaisant à 60V.
Liste des composants utilisés (commandés sur les sites internet indiqués. Dernière consultation 13/06/2016)
– Pile Bouton : http://www.ruedespiles.com/piles-boutons/pile-bouton-3v-cr/pile-cr-2032-varta-3v-lithium-par-1-p-14104.html?ggs&gclid=CO2vyO7wq8oCFRFmGwodXU0Gww
– Relais : http://fr.farnell.com/te-connectivity-axicom/5-1462037-3/relais-de-signal-dpdt-250vac-220vdc/dp/2251783
– Diodes : http://fr.farnell.com/fairchild-semiconductor/1n4149/small-signal-diode-500ma-direct/dp/1651147
– Bobines : http://www.conrad.fr/ce/fr/product/440339/Inductance-Fastron-77A-682M-00-sortie-axiale-6800-H-96-1-pcs
– Condensateurs : http://www.conrad.fr/ce/fr/product/453064/Condensateur-ceramique-10-nF-50-V-10-1-pcs
– Résistance variable : http://www.conrad.fr/ce/fr/product/430730/Trimmer-Piher-PT-10-LH-10K-miniature-linaire-015-W-10-k-220-240-1-pcs?ref=list
– Transistor : http://fr.farnell.com/fairchild-semiconductor/bs170/transistor-mosfet-n-to-92/dp/1017687
– Trigger de Schmitt : http://fr.farnell.com/texas-instruments/cd4093bm/trigger-schmitt-logique-nand-soic/dp/2395910
Nanoparticules d’or en catalyse organique
Tippe Top, la toupie renversante
Les programmes Matlab réalisés pendant les PSE sont disponibles sur simple demande par mail:
antoine.rideau@espci.fr
(Impossible d’uploader ce type de fichier sur WordPress)
Nanoparticules et stockage d’énergie
MESURES DE LA REPONSE ELECTROCHIMIQUE DE CoNRs EN SUSPENSION
Matériel :
– Une microélectrode d’or (« faite maison »)
– Une contre électrode en graphite.
– Electrode de référence en argent
– Cage de Faraday (ici boîte en carton emballé dans de l’aluminium).
– Support/socle de mousse polymère.
– Potentiostat « CH Instruments ».
– Solutions de CoNPs, une pour chaque surfactants utilisés dans la préparation selon notre protocole (cf « Préparation suspension CoNPs »)
Protocole :
Pour chaque solution : mesure sur un blanc (solution + surfactants sans CoNRs) et sur la solution d’intérêts.
– On effectue d’abord une ou plusieurs mesures de cycle voltamètrique. En comparant les mesures du blanc et de la solution d’intérêt on repère le potentiel d’oxydation du cobalt en solution
– On effectue alors ensuite, pour le blanc et la solution d’intérêt, une mesure de chronoampèromètrie, on aura alors pris soin de se placer au potentiel d’oxydation du cobalt en solution mesuré précédemment.
– On repère alors sur les courbes chronoampèromètriques tous ce qui peut s’apparenter à un signal dû à la réponse électrochimique d’une CoNP entrant en contact avec l’électrode. On distingue différent type de pics : des « paliers », des « Dirac » et des « gaussien » (c’est appellation ne représente que la forme des pics sans aucune justification mathématique). Ordre de grandeur 10pA pendant 0.2ms
– On référence alors ces signaux selon leurs types, leurs durées et leurs intensités pour chaque expérience. On en déduit alors par l’intensité et la durée une estimation de la charge transférée par CoNP. On estime alors la fréquence de collision ce qui nous permet de remonter à la taille moyenne d’une CoNP de notre solution et du coefficient de diffusion.
Paramétrage :
– Voltamétrie :
potentiel initial : 0V
potentiel max : 2,1V
potentiel min : 0V
vitesse de mesure : 0,1 V/s
segment : 2
intervalle de mesure entre deux points : 0,001V
quiet time : 2s
sensibilité : 5.10-8A/V
– Chronoampèrométrie :
potentiel initial : 0V
potentiel max : potentiel oxydation CoNR mesurée pour la solution
potentiel min : 0V
Init P/N = P
Step : 1
Pulse Width (sec) = 500
Sample Interval (s) = 0.1
Quiet Time (sec) = 2
Sensibilité : 10-9 A/V
METHODE POUR ETUDIER LA CATALYSE DE LA DISMUTATION DE L’EAU AU NIVEAU D’UNE NANOPARTICULE UNIQUE
Qu’est-ce que l’électrolyse de l’eau ?
C’est le processus électrolytique par lequel l’eau liquide forme du dihydrogène et du dioxygène gazeux.
Cette réaction est défavorable d’un point de vu thermodynamique puisque les potentiels standards de réaction traduisent que la réaction inverse est spontanée et l’enthalpie libre de cette réaction est fortement positive (474kJ).
Pourquoi catalyser avec des nanoparticules de cobalt ?
Certains matériaux constituants les électrodes des cellules électrochimiques permettent d’abaisser cette barrière énergétique par leurs états de surface et leurs capacités à conduire les électrons. C’est le phénomène de surtension. Ici nous étudions des nanoparticules de cobalt car ce matériaux possède des propriétés catalytiques connues pour cette réaction et les nanoparticules possèdent un rapport surface/ volume important ce qui permet de maximiser la surface catalytique et donc le rendement de la réaction.
Pourquoi catalyser cette réaction ?
La catalyse de l’électrolyse de l’eau s’inscrit dans une problématique plus globale de diversification des sources d’énergie car elle rentre dans une logique d’optimisation de la production d’hydrogène.
La ressource hydrogène peut être utilisée pour alimenter des piles à combustible. Celles-ci consomment du dihydrogène et du dioxygène et rejettent de l’eau. Et la production d’hydrogène à partir d’eau est le processus le plus propre d’un point de vu chimique. Ce couple de technologie qui utilise l’eau dans un cycle pour créer de l’énergie est une solution d’avenir pour certaines applications.
Cependant, on a vu précédemment que la réaction d’électrolyse de l’eau est défavorable et donc, le coup énergétique de production d’hydrogène par électrochimie reste encore inintéressant pour des applications industrielles.
En quoi consiste notre étude ?
On veut mettre en place une méthode pour étudier la catalyse de l’électrolyse de l’eau à l’échelle de la nanoparticule unique. Cela permettra de déterminer les processus chimique et la cinétique de catalyse pour être capable d’optimiser la composition et la taille des nanoparticules. En effet le but final est d’avoir une méthode robuste pour étudier des nanoparticules en masse.
Plus précisément on veut suivre et mesurer la taille des nanoparticules par holographie et mesurer leurs réponses électrochimiques au contact d’une microélectrode.
Comment étudier la réponse électrochimique d’une seule nanoparticule ?
On réalise une cellule de mesure électrochimique classique composé de d’une microélectrode de mesure en or et une électrode de référence en argent. L’électrolyte est constitué d’une suspension de nanoparticules de cobalt stabilisé par un surfactant (PVP) et d’un tampon au phosphate (pH 7).
Remarque : Le phosphate est nécessaire spécifiquement dans la réaction de catalyse par le cobalt
La petite taille de l’électrode permet statistiquement de détecter les impacts de nanoparticule dessus une par une. Un voltamètre nous permet de mesurer le courant produit lors de l’électrolyse qui est de l’ordre du picoampère.
On peut réaliser diférents type de mesures :
*courbes intensité potentiel : elles permettent de mettre en évidences les propriétés catalytiques des particules utilisées.
*chronoampérométrie (intensité en fonction du temps) : en se plaçant à un potentiel tel qu’il ait électrolyse qu’en présence d’une nanoparticule sur l’électrode on peut détecter des impacts de nanoparticule et étudier leur réponse électrochimique.
PREPARATION SUSPENSION CoNPs
Liste matériel :
• CoNPs (nanoparticules de Co) en poudre :Sigma Aldrich CAS Number 7440-48-4
• Phosphate Buffer Saline: Sigma Aldrich MDL number MFCD00131855
∞ surfactants : PvP, SDS, triton, tween 80, tween 20 …
∞ bain à ultrasons
∞ centrifugeuse
Protocole :
Pour chaque surfactant :
Mettre 5g de CoNRs en poudre dans 10 mL d’eau avec environ 1% en masse de surfactant soit une goutte ou une pointe de spatule selon le surfactant.
Plonger alors la suspension dans le bain à ultrason afin de briser les agrégats par sonication, temps d’exposition : environ 5min. Une deuxième exposition peut être envisager si la première ne semble pas avoir été assez efficace.
Attention cependant à ne pas reproduire la sonication trop souvent ou de laisser un temps d’exposition excessif : cela aurait pour risque d’endommager les nanoparticules.
Si l’on souhaite éliminer les agrégats les plus gros on peut aussi centrifuger notre solution pour n’en prélever que le surnageant mais on perd alors l’information sur la concentration.
MESURES DE LA REPONSE ELECTROCHIMIQUE D’UN DEPOT DE CoNRs SUR UNE ELECTRODE
Dépot sur électrode de graphite :
Matériel :
– morceau de feuille de graphite. Dimension : 2x3cm [fournisseur + prix]
– « parafilm « M » » (film de paraffine ). Dimension : 2×2.5 cm
– plaque chauffante
– solution de nanoparticule
Protocole :
cf schéma
Dépot sur ultramicroélectrode :
Matériel :
– micro-électrode d’or.
– cône pour micropipette [quelle calibre]
Protocole :
cf schéma
Paramètres pour les cycles voltamétriques :
Les mesures sont effectuées avec un potentiostat.
Comme nos mesures sont très sensibles, on pourras diminuer le bruit dû aux vibrations mécanique en posant notre dispositif sur un bloc de mousse (ammortissement des chocs), et le bruit électrique en plaçant le dispositif à l’intérieur d’une cage de Faraday.
Paramêtres de mesures :
-potentiel initial : 0V
-potentiel max : 2,1V
-potentiel min : 0V
-vitesse de mesure : 0,1 V/s
-segment : 2
-intervalle de mesure entre deux points : 0,001V
-quiet time : 2s
-sensibilité : 5.10-4A/V
On comparera nos mesures faites sur les électrode avec dépôts par rapport au mesures faites sur des électrodes témoins (sans dépôt de CoNRs).
CARACTERISATION CoNRs PAR DLS
Principe :
La diffusion dynamique de la lumière (DLS) est une technique d’analyse spectroscopique non destructive permettant d’accéder à la taille de particules en suspension dans un liquide ou de chaînes de polymère en solution de 1 à 500 nm de diamètre environ.
Lorsque la lumière d’un laser atteint des petites particules dans une microcuvette, la lumière diffuse dans toutes les directions. Ce phénomène est principalement de la diffusion de Rayleigh, diffusion élastique où les particules sont plus petites que la longueur d’onde considérée. On peut mesurer l’intensité de la lumière diffusée par les particules à un angle considéré (90° typiquement) au cours du temps. Cette dépendance en temps vient du fait que les particules dans un liquide sont soumises au mouvement brownien à cause de l’ agitation thermique. La distance entre diffuseurs (concentration locale) change ainsi sans cesse. Il en résulte des interférences constructives ou destructives et l’intensité totale mesurée contient des informations sur la vitesse de mouvement des particules.
Protocole :
-On place dans des microtubes de 2mL 40 mg de nanoparticules de Cobalt commerciales pesée à la balance de précision, étant donnée la quantité considérée et vu que l’on met les Nps dans les microtubes avec une spatule la précision sur la masse est faible, pareil pour le surfactant
– On met une goutte de surfactant .
Liste des surfactants testés : – SDS
– PEG
– Tween 20
– Tween 80
– SLS
– Triton X-100
– POEA
– Cocamidopropyl betaïne
– On complète avec de l’eau MilliQ jusqu’ à 2mL, on obtient une solution inhomogène avec de gros agrégats dispersés en solution et un dépôt
– On mélange gràce à un vortex pour casser les gros agrégats et homogénéiser la solution puis on passe les microtubes au bain à ultrasons pour casser les plus petits agrégats. On remarque que la couleur varie d’une solution à l’autre en fonction du surfactant utilisés.
– On passe les microtubes à la centrifugeuse à 5000tours/min, il ya formation d’un culot, on prélève le liquide surnageant.
– On met les solutions dans une microcuve spéciale pour la DLS
– On lance le protocole préprogrammée de la DLS
On récupère alors une intensité normalisée en fonction de la taille.
Remarque :
Etant donnée la quantité considérée et vu que l’on met les Nps dans les microtubes avec une spatule la précision sur la masse est faible, pareil pour le surfactant